��������ڰµ�ƽƬ������ҩ������ѧ�������Ч��
���ı� ����Ծ ������ ������ ������
����ҽ�ƴ�ѧ������������ҽԺ�ٴ�����ҩ��ʵ���ң����� 100088 ��
[ժҪ] Ŀ�ģ����콡�������߿ڷ��µ�ƽƬ��ҩ������ѧ���ȽϹ����Ƽ�������Ƽ��������Ч�ԡ�
������ ����˫�������Ƽ�����������ƣ��� 22 �����Խ���־Ը�������Ϊ���飬���浥�μ����ڷ���������ڰµ�ƽƬ
10mg ���ø�ЧҺ��ɫ�绯ѧ��ⷨ�ⶨ��ҩ��ͬʱ���Ѫ���аµ�ƽ��Ũ�ȣ����� 3P97 �Ƿ���ģ�ͷ������Ч�Լ���������ͳ�Ʒ�����
����� ���οڷ������ͽ��ڰµ�ƽƬ���ѪҩŨ��ʱ���������ƣ���Ҫҩ������ѧ����Cmax �ֱ�Ϊ��20.77��4.86���ͣ�19.31��4.80��
��g��L-1 �� T max �ֱ�Ϊ��2.91��0.68���ͣ�3.73��1.24�� h �� AUC
0 �� 144 �ֱ�Ϊ��643.94��156.35���ͣ�636.53��187.19�� ��g��h��L-1
�� AUC 0 �� �� �ֱ�Ϊ��688.42��156.19���ͣ�684.85��192.66�� ��g �� h �� L-1
�������µ�ƽƬ�Խ��ڰµ�ƽƬ������������ö� F-AUC 0 �� 144 Ϊ��105.2��25.0�� % �� F-AUC
0 �� �� Ϊ�� 104.8��27.9 �� % ���� T max �⣨P��0.05 ����Ҫҩ������ѧ���� C max
�� AUC 0 �� 144 �� AUC 0 �� �� ���������Բ��죨P��0.05����
���ۣ� �����ͽ��ڰµ�ƽƬ���������Ч�ԡ�
[�ؼ���] �µ�ƽ
ҩ������ѧ �����Ч�� Ƭ�� ��ЧҺ��ɫ�� �绯ѧ��ⷨ
Human pharmacokinetics and bioequivalence
of domestic and imported
olanzapine tablets
LI Wen-biao, WANG Chuan-yue, ZHAI Yi-min,
WENG Yong-zhen and JIANG Zuo-ning
(Laboratory of Clinical Psychopharmacology, Beijing Anding
Hospital, Affiliate of the Capital University of Medical Sciences,
Beijing 100088, China)
�� Abstract �� Objective :
To study the pharmacokinetics of olanzapine tablets
after oral administration, compare the bioequivalence of domestic
and imported olanzapine tablets. Methods:
22 male volunteers received an oral single-dose of 10mg domestic
and imported olanzapine tablets respectively by a randomized
2way crossover design. The plasma olanzapine concentrations
of deferent time were determined by high-performance liquid
chromatography with electrochemical detection. The pharmacokinetic
parameters of olanzapine and the bioequivalence of the two
formulations were evaluated by 3P97 program. Results:
The plasma drug concentration��time curves of the
two formulations were very similar. The main pharmacokinetic
parameters of both domestic and imported were given respectively
as following: C max were (20.77��4.86) and (19.31��4.80)��g ��
L-1 �� T max were (2.91��0.68) and (3.73��1.24)h ��
AUC 0 �� 144 were (643.94��156.35) and (636.53��187.19) ��g��h��L-1
�� AUC 0�u�� were (688.42��156.19) and (684.85��192.66) ��g��h��L-1
�� The relative bioavailability of domestic to imported tablets
were: F-AUC 0 �� 144 = �� 105.2��25.0 �� % �� F-AUC 0 �� �� = �� 104.8��27.9
�� % �� No significant deference was found for the pharmacokinetic
parameters C max , AUC 0 �� 144 and AUC 0 �� �� (P �� 0.05), except
T max (P �� 0.05). Conclusion: Domestic
and imported olanzapine tablets are of bioequivalence.
[ key words ] olanzapine; pharmacokinetic;
bioequivalence; HPLC; electrochemical detection
�µ�ƽ (Olanzapine) Ϊ���ͷǵ��Ϳ�����ҩ���ѧ�ṹ���ȵ�ƽ���ƣ�ҩ�����ý��ƣ����ھ������֢���˵�����֢״������֢״����������Ч����������������ϵ��Ӧ����Ѫ�������ˮƽӰ��С����������ϸ��ȱ��֢
[1~2] ���µ�ƽ���Ͱ� D 1 �� D 2 �� D 4 ���壬 5- ��ɫ�� 5-HT 2a �� 5-HT 2c
�� 5-HT 3 ���壬 a 1 ���壬 H 1 ���壬 M ���������һ���������������� D 2 ������������������ȵ�ƽǿ����
N- ����������ϡ�ͬ���ðµ�ƽ�йص���Ҫ������Ӧ����˯���������ӣ�ż����ҩ���ڳ��ָ���ת��ø SGPT �� SGOT
һ����������ߡ�Ŀǰ���ҹ����е���Ҫ������������˾�����ݵ�ƽƬ�������ڼ۸����ಡ�����Գ��ܡ������µ�ƽƬ���ɹ���ʳƷ��ҩƷ�ල�����������С�������µ�ƽ���й������Խ���־Ը�����ڵ�ҩ������ѧ�������о������ұȽ��˹����µ�ƽƬ��������������˾�����ݵ�ƽƬ���������Ч�ԡ�
�����뷽��
1. ҩƷ���Լ�
�����Ƽ�Ϊ���ݻ�����ҩ����˾�����ݵ�ƽƬ������� 5 mg/ Ƭ������ 20000709 ��ҩ��ϸα��Ƽ�Ϊ����������˾�����ݵ�ƽƬ������Ʒ�������֣�
Zyprexa ������� 5 mg/ Ƭ������ C5358C ���µ�ƽ���ڱ��һ��µ�ƽ��Ʒ�ɳ��ݻ�����ҩ����˾�ṩ�����Ⱦ�
��99.9% ��ά���� C �������� Sigma ��˾���״�������Ϊ����ɫ�״��Լ������ѡ��������ء���������ơ���ˮ̼���ơ����ᡢ���ȶ���������Լ���Ϊ���۷����������۷����������辭������һ����ʹ�á�����Ϊ�ߴ������հ�Ѫ��Ϊ������֮���Ѫ����
2. ����
���� L-6200 ��ЧҺ��ɫ�ױã����� BIO-RAD1640 �͵绯ѧ����������� D-2500 ��ɫ�����ǡ�����Ԥ���������Թܼ���������������辭���ȶ�������軯��ʹ�á�
3. ���Զ���
22 ����������������ƽ�����䣨 24.91��5.67 ���꣬ƽ�����أ� 65.32��9.91 �� Kg ��ƽ�����ߣ�
170.95��5.78 �� cm ���������������ش�ʷ�������Ѫѹ��������������Ѫ�桢�������ܡ��ĵ�ͼ�ȷ�������쳣���֡�����ǰ���ܼ������ڼ�δ������ҩ������ڼ�����̡��Ƽ�������������ϡ����������߾���Ը���ܱ����飬ǩ��֪��ͬ���顣
4. ��ҩ����
����˫�������Ƽ�����������ơ��� 22 ���������������Ľ���־Ը�߰�������ֱ�����Ϊ A �� B ���飬ÿ�� 11
�������������߷ֱοڷ����Ի�αȰµ�ƽƬ 10mg ����ʱ��Ѫ����Ѫ�������� 3 �ܣ�Ȼ���ҩ���ظ����顣�������ڷ�ҩǰ
1 �������ס��������ʳ 12 Сʱ����ҩ�����峿�ո����μ����ڷ���������ڰµ�ƽƬ 10mg �����¿�ˮ 250ml
�̷��� 2 Сʱ������֬����ʳ�������߷�ҩǰһ�����������ҩ�� 2 ���ڽ���ͳһ�ĵ�֬�����ͣ��Ժ��Ϊ��ͨ��ʳ��
5. Ѫ���ɼ�
���������߷ֱ��ڷ�ҩǰ�ͷ�ҩ��� 1 �� 2 �� 3 �� 4 �� 6 �� 8 �� 12 �� 24 �� 36 �� 48
�� 72 �� 96 �� 120 �� 144 Сʱ��ȡǰ�۾���Ѫ 5ml ������ͳһ�ĸ��ػ��Թ��У��������ȣ� 4000rpm
���� 5min ����Ѫ����ȡ˫�ݸ� 1ml Ѫ�������ں��� 0.1mol �� L -1 ��ά���� C ��Һ 0.5ml
�� Eppendorf ���У����ȣ� -20 �� C ���棬ͳһ�ⶨ��
6. �ٴ��۲�
���������������ҽ�ƴ�ѧ������������ҽԺ����ҽ����Ա���м�½��С������߷��ðµ�ƽ��ʱ�۲����¼Ѫѹ�����������������ºͲ�����Ӧ����д������Ӧ�ǼDZ�����ҩ��סԺ�۲�
2 �죬�Ժ�����ɻ���ϸ�ʱ��Ѫ�����һ�β�Ѫʱ������Ѫ�����������������ܣ���
7. ѪҩŨ�Ȳⶨ����
���ø�ЧҺ��ɫ�绯ѧ��ⷨ�ⶨѪ�������аµ�ƽ��Ũ�ȡ��������������η�ҩ��ɼ�����������ͬһ���ڲⶨ��ÿ���ⶨ��ͬһ����ɣ����õ��ձ����ߣ�ͬʱ�ⶨԤ��ͳһ���Ƶݵ�ƽŨ��Ϊ
1 �� 8 �� 32 m g��L -1 ���ʿ�Ѫ����һ�ݡ�
7.1 ɫ������ ɫ����Ϊ Inertsil ODS-3 �� 5 m m �� 4.6mm��150mm ���ձ� GL
Science ����������Ϊ�״� : ���� : ����ˮ :50mmol �� L -1 KH 2 PO 4 ��Һ :50mmol
�� L -1 Na 2 HPO 4 ��Һ�� 32:26:8:20:14 �ı�����ϣ��� 0.45 m M ����Ĥ��ѹ���˶��ɣ�����Ϊ
2.0ml �� min -1 ���绯ѧ������ļ���ѹΪ 0.32V �������� 10nA �� V -1 ������ 0.15V
��������ֽ�� 0.25cm �� min -1 ��
7.2 Ѫ����ƷԤ���� ����Ѫ�� 1ml ���뺬�� 0.1mol �� L -1 ά���� C ��Һ 0.5ml ���Թ��У�����Ũ��Ϊ
160 m g��L -1 ���ڱ� LY170222 �״���Һ 50 m l �����ȣ��ټ��� 1mol �� L -1
�� Na 2 CO 3 ��Һ 0.5ml ���������� 4ml �����л�� 2min �� 4000 r��min -1
���� 5min ��ȡ���ϲ����ѣ� 40 �� C ˮԡ�µ������ɣ����������� 50 m l �ܽ⣬ 4000r��min
-1 ���� 5min ��ȡ 25 m l ������
7.3 �������Ʊ� 1ml �հ�Ѫ�� 8 �ݣ����ηֱ����״���Ũ��Ϊ 10 �� 20 �� 40 �� 80 ��
160 �� 320 �� 640 m g��L -1 �ݵ�ƽ���״���Һ 50 m l ���ðµ�ƽŨ�ȷֱ�Ϊ 0 ��
0.5 �� 1 �� 2 �� 4 �� 8 �� 16 �� 32 m g��L -1 ��ϵ��Ѫ��Һ�������� 0.1mol ��
L -1 ��ά���� C ��Һ 0.5ml �����ȣ��� 7.2 �������������д������µ�ƽ���ڱ�ķ�߱���µ�ƽŨ�Ƚ������Իع飬��������ߡ�
8. ���ݷ���
�����й�ҩ��ѧ����ѧרҵίԱ����Ƶ� 3P97 �Ƿ���ģ�ͷ������Ч�Լ���������ͳ�Ʒ����������η����������Ƽ����Ե�
AUC 0 �� 144 �� AUC 0 �� �� �� C max �� T max ����ʵ��ֵ���Է��������˫���� t
����� 90% �������䣬���������Ƽ��������Ч�ԡ�
�� ��
1. ѪҩŨ�Ȳⶨ����������
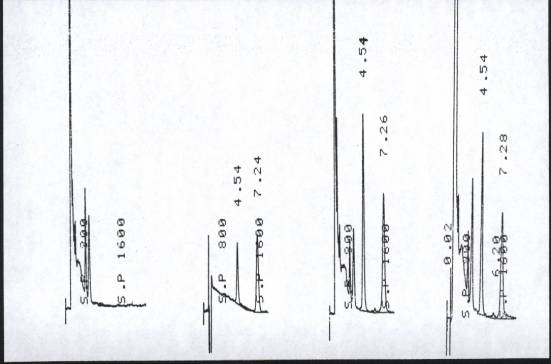
1.1 ɫ��ͼ�������� �µ�ƽ���ڱ�ı���ʱ��ֱ�Ϊ 4.54min �� 7.26min �����߷������ã�������ȫ����Դ�����ʺͰµ�ƽ��л����������������ⶨ����ͼ
1 ��
 ͼ
1. ɫ��ͼ �µ�ƽ����ʱ�� 4.54min �ڱ걣��ʱ�� 7.26min ͼ
1. ɫ��ͼ �µ�ƽ����ʱ�� 4.54min �ڱ걣��ʱ�� 7.26min
A ���հ�Ѫ�� B �����µ�ƽ 40 m g��L -1 ���ڱ� 80 m g��L -1 �ı��״���Һֱ�ӽ���
C �����µ�ƽ 8 m g��L -1 ���ڱ�ı�Ѫ�� D ��־Ը�߷�ҩ��Ѫ��
Fig 1. Chromatogram The retention time of olanzapine and
internal standard is 4.54min and 7.26min
A �� blank plasma; B �� director injection of 40 m g��L -1 olanzapine
and 80 m g��L -1 internal standard in methnol; C �� plasma of
8 m g��L -1 olanzapine and internal standard; D �� plasma of
a volunteer after oral dose.
1.2 �����������Թ�ϵ �� 0.5 �� 32 m g��L -1 �ķ�Χ�ڣ��µ�ƽ������ڱ���֮�ȺͰµ�ƽѪ��Ũ��֮��������õ�ֱ����ع�ϵ�������ߵ����Է���Ϊ��
y=-0.00296+0.19720x �� r=0.9993 ������ y Ϊ�µ�ƽ���ڱ�ķ�߱ȣ� x ΪѪ���µ�ƽŨ�ȡ�
1.3 �����ʺ;��ܶ� �ÿհ�Ѫ�����ưµ�ƽ�궨Ũ��Ϊ1��8��32 m g �� L -1 ���ڱ�Ũ��Ϊ8 m g
�� L -1 ��Ѫ����������7.�����ⶨ���Ժ�ҩѪ������ȡ���õ�ɫ�������ӦŨ��ҩ��״���Һֱ�ӽ�����ɫ��ߵİٷֱ�Ϊ���Ի����ʣ��µ�ƽ���Ũ����궨Ũ�ȵİٷֱ�Ϊ��Ի����ʣ��������1��6�ݺ�8
m g �� L -1 �ڱ�Ѫ��ⶨ���ڱ���ȡ������Ϊ85.05 �� 2.08%��RSDΪ2.47%��
�� 1 ����ЧҺ��ɫ�绯ѧ��ⷨ�ⶨ�µ�ƽѪ��Ũ�ȵĻ����ʺ;��ܶ�
Table 1. Recovery and accuracy for the determination of plasma
olanzapine concentration by high-performance liquid chromatography
with electrochemical detection
Ũ�� / m g��L -1 |
��Ի����� /%
(n=6) |
���Ի����� /%
(n=6) |
���� RSD/%
(n=6) |
�ռ� RSD/%
(n=22) |
1 |
108.17��3.06 |
85.28��4.78 |
2.78 |
10.21 |
8 |
105.21��6.69 |
80.42��4.59 |
6.29 |
9.22 |
32 |
104.39��8.58 |
81.25��5.59 |
8.34 |
8.91 |
2. ѪҩŨ�� �� ʱ������
22 ������־Ը�ߵ������ڷ������ͽ��ڰµ�ƽƬ 10mg ���ƽ��ѪҩŨ�� �� ʱ������ͼ 2 ��
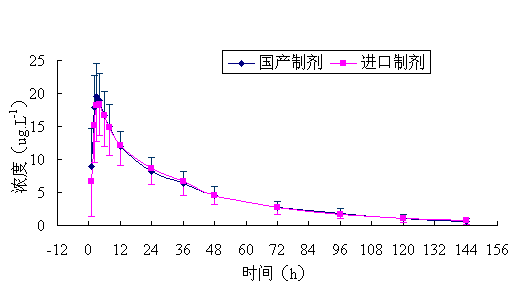
ͼ 2. 22 �����Խ���־Ը�ߵ������ڷ������ͽ��ڰµ�ƽƬ 10mg ���ƽ��ѪҩŨ�� �� ʱ������
Fig 2. Mean plasma concentration-time curves of domestic
and imported olanzapine tablets after a single oral dose in
22 healthy male volunteers.
3. ��Ҫҩ������ѧ����
���� 3P97ͳ�����������22�����������ߵ������ڷ��µ�ƽ10mg����Ҫҩ������ѧ��������2��
�� 2 ���������ڷ������ͽ��ڰµ�ƽƬ�������Ҫҩ������ѧ����
Table 2. Main pharmacokinetic parameters of domestic and
imported olanzapine tablets after a single oral dose.
�� �� |
����Ƭ�� |
����Ƭ�� |
AUC 0 �� 144 /��g �� h �� L -1 |
643.94��156.35 |
636.53��187.19 |
AUC 0 �� �� /��g �� h �� L -1 |
688.42��156.19 |
684.85��192.66 |
C max / m g��L -1 |
20.77��4.86 |
19.31��4.80 |
T max /h |
2.91��0.68 |
3.73��1.24 |
T 1/2ke /h |
36.78��8.80 |
33.67��7.20 |
MRT 0~t /h |
36.32��4.41 |
34.90��5.96 |
MRT 0~ �� /h |
46.77��8.66 |
45.80��9.54 |
4. �����Ч���ж�
���µ�ƽƬ����������ö� F-AUC 0 �� 144 Ϊ�� 105.2��25.0 �� % �� F-AUC 0 ��
�� Ϊ�� 104.8��27.9 �� % ��������Ƭ���� AUC 0
�� 144 �� AUC 0 �� �� �� C max ���з��������˫������鼰 90% �������죬���������Ƽ����������Ч�ԣ�����
3 �������Ⱥͼ���Ľ���������µ�ƽƬ����ʵ�� T max ���ڲα�Ƭ���� Z=-2.428 �� P �� 0.05
��
�� 3 �������ͽ��ڰµ�ƽƬ���������Ч�Է���
Table 3. Bioequivalent analysis of domestic
and imported olanzapine tablets
�� �� |
T 1 |
T 2 |
P ֵ |
90% ������ |
ln AUC 0��144 |
5.539 |
4.282 |
0.5364 |
95.1~111.3 |
ln AUC 0���� |
5.141 |
4.251 |
0.6614 |
94.1~110.9 |
lnC max |
6.959 |
3.351 |
0.0863 |
100.3~116.5 |
5. ������Ӧ���
22 �������߷������ԺͲαȰµ�ƽƬ�����ֲ�ͬ�̶ȵ���˯��������Ϊ 100% ������������Ӧ��ͷ�Ρ��Ķ��������Ķ����١���λ�Ե�Ѫѹ���ڸɡ������Ͷ��ġ���Щ������Ӧ�������أ����账��������Ȼ���⣨����
4 ����
�� 4 �� 22 ��־Ը�ߵ������ڷ���������ڰµ�ƽƬ��IJ�����Ӧ
Table 4. Adverse reactions of domestic and imported olanzapine
tablets after a single oral dose in 22 volunteers
������Ӧ
�� �� |
����Ƭ��������
( ������ ) |
�α�Ƭ��������
( ������ ) |
˵ �� |
��˯
|
22
(100%) |
22
(100%) |
���ڷ�ҩ�� 1-4 Сʱ���֣�Ϊ��ȵ��жȣ����� 8~12 Сʱ�������ʧ�� |
ͷ��
|
7
(31.82%) |
7
(31.82%) |
�����ڷ�ҩ�� 4~12 Сʱ���ᵽ�ж� |
�Ķ�����
|
3
(13.64%) |
6
(27.28) |
���� 46~60 �� /min �����ڷ�ҩ�� 4~8 Сʱ������ 1~2
Сʱ |
�Ķ�����
|
2
(9.09%) |
3
(13.64%) |
�����ڷ�ҩ�� 8~36 Сʱ������ 100~110 �� / �֣����� 1~2
Сʱ |
��λ�Ե�
Ѫѹ |
2
(9.09%) |
1
(4.55%) |
Ѫѹ���� 95/50mmHg �����ڷ�ҩ�� 4~8 Сʱ |
����
|
1
(4.55%) |
2
(9.09%) |
�����ڷ�ҩ�� 1~12 Сʱ����ȵ��ж� |
�ڸ�
|
1
(4.55%) |
1
(4.55%) |
�����ڷ�ҩ�� 1~12 Сʱ����ȵ��ж� |
����
|
1
(4.55%) |
0
|
��ʱ����� |
�� ��
�ѱ����ݵ�ƽѪҩŨ�Ȳⶨ����������ЧҺ��ɫ������ⷨ [3-5] �������ⷨ [6-8] �͵绯ѧ��ⷨ [9-10]
�ȡ����ڰµ�ƽ���ռ�����Ϊ 5 �� 20mg [ 1-2 ] �����ƾ������֢����ЧѪ����Ũ��ԼΪ 9 m g��L
-1 [ 9 ] �������ⷨ�������ȿ�����������ҩ�������Ҫ������������ҩ������ѧ�о���Ҫ������ⷨ���������������Dzο�
Aravagiri �� [ 9 ] �� Catlow �� [ 10 ] �ķ������ҹ����Ƚ����˲ⶨ�µ�ƽŨ�ȵĸ�ЧҺ��ɫ�绯ѧ��ⷨ
[ 11 ] �����������ȸߡ�������ǿ���������ŵ㡣��������ķ���һ�ν���������Ҫ 15 ���ӣ���Ϊ��ʱ�����ڱ�����������ⶨ���ϴ����Ǹ�������ԭ����ͬ�ͺŵĶ�ɫ��������������������˵�����ʹһ�ν����ķ���ʱ������Ϊ
9 ���ӣ������������˷�������Ч�ʡ����о����òⶨ������ 2000 ��桶�й�ҩ�䡷 [ 12 ] ��Ҫ�������ⶨ���ϸ�����������½��С�
�µ�ƽ���й������ڵ�ҩ������ѧ�о���δ���������ݹ��� Nyhart �� [ 13 ] �������ڷ��µ�ƽƬ�� 15mg
��ƽ�� C max �� T max �� AUC 0~ �� �� T 1/2ke �ֱ�Ϊ 13.45 m g��L -1
�� 5.9h �� 498��136��g �� h �� L -1 �� 29.1��5.8h ���ݹ������� [ 3 ] �������µ�ƽ�ڷ���
5~8h �ﵽѪ����ֵŨ�ȣ�ƽ��������˥��Ϊ 33h(5% �� 95% Ϊ 21 �� 54 Сʱ ) ����������������
22 ��־Ը�߿ڷ� 10mg ���ԺͲαȰµ�ƽƬ���� C max �ֱ�Ϊ 20.77��4.86 �� 19.31��4.80
m g��L -1 �� T max �ֱ�Ϊ 2.91��0.68 �� 3.73��1.24h �� t 1/2ke �ֱ�Ϊ
36.78��8.80 �� 33.67��7.20h �� AUC 0 �� 144 �ֱ�Ϊ 643.94��156.35 ��
636.53��187.19��g �� h �� L -1 �� AUC 0 �� �� �ֱ�Ϊ 688.42��156.19 ��
684.85��192.66��g �� h �� L -1 ���ɼ� C max �� T max �� AUC 0~�� �����ױ�����ֵ�нϴ��𣬵���
T 1/2ke �����Բ����ʾ�й��˿ڷ��µ�ƽ�����սϿ죬��Ũ�Ƚϸߣ��п���ʹ�ýϵ͵��ռ��������ֲ�����������������ؽ��ἰ��л����IJ����йأ��д���һ���о���
�����µ�ƽƬ�Խ��ڰµ�ƽƬ������������ö� F-AUC 0 �� 144 Ϊ�� 105.2��25.0 �� % �� F-AUC
0 �� �� Ϊ�� 104.8��27.97 �� % ������ 3P97 �����Ч�Լ���������ְµ�ƽƬ���������η������
AUC 0 �� 144 �� AUC 0 �� �� ��ʵ�� C max �� T max �� T 1/2ke ���ж����ط��������˫����
t ���飬�����������Ƭ���� AUC 0 �� 144 �� AUC 0 �� �� �� C max �� T 1/2ke ���������Բ��죨
P �� 0.05 ���� t 1 �� t 2 ֵ������ 1.725 ������Ƭ�� AUC 0 �� 144 �� AUC 0
�� �� ������ת����ֵ�� 90% �Ŀ�������ֱ�Ϊ 95.1% �� 111.3% �� 94.1%~110.9%
�� C max ������ת���������Ƽ���ֵ�� 90% �Ŀ�������Ϊ 100.3% �� 116.5% �����Ͻ�������ҹ�ҩ���ж������Ч�Ե�Ҫ��
[12] ���ʿ���Ϊ�����µ�ƽƬ����ڰµ�ƽƬ��������������Ч�ԡ����������˫���� t ����Ľ�����������µ�ƽƬ��
T max ���ڲαȰµ�ƽƬ (P �� 0.05, t 1 �� 1.725 ) , ��ʾ���ݻ�����ҩ��˾�����ݵ�ƽƬ��������սϿ죬�����������ٴ����塣
��������۲쵽�IJ�����Ӧ��Ҫ����˯���������������߷������ԺͲαȰµ�ƽƬ����е���ͬ�̶ȵ����룬����µ�ƽ�������ü���ҩ���Դ���Ϣ�йأ����⽡���˱Ⱦ������֢���˶µ�ƽ���ܸ�Ϊ���С�����������Ӧ��ͷ�Ρ��Ķ��������Ķ����١���λ�Ե�Ѫѹ���ڸɡ������Ͷ��ġ���Щ������Ӧ�������أ����账��������Ȼ���⡣�ں��������¡��ĵ�ͼ��
B ����Ѫ������Ѫ��ȷ�������쳣���֡�
[ ����� ] ���ı꣨ 1963- �����У�ҽѧ˶ʿ�������μ�ʦ����Ҫ�����ٴ�����ҩ��ѧ�о���������ϵ�绰����
010 �� 82085468 �� 82085467 �� E-mail: swbli@sina.com
��
�����
[1] ���� , ��ƽ . ���ͷǵ��Ϳ�����ҩ�µ�ƽ . �л��������־ , 1999, 32 (4): 123.
[2] ½���� , Ԭ���� . ��һ�����������֢ҩ��µ�ƽ . �й���ҩ��־ , 1999, 8(3) : 161.
[3]Berna M, Shugert R, Mullun J. Determination of olanzapine
in human plasma and serum by liquid chromatography/tandem
mass spectrometry. J. Mass Spectrom., 1998, 33: 1003-1008.
[4]Bogusz MJ, Kruger KD, Maier RD, et al. Monitoring of olanzapine
in serum by liquid chromatography-atmospheric pressure chemical
ionization mass spectrometry. J Chromatogr B, 1999, 732: 257-269.
[5]Berna M, Ackermann B, Ruterbories K, Glass S. Determination
of olanzapine in human blood by liquid chromatography-tandem
mass spectrometry. J Chromatogr B Analyt Biomed life Sci.
2002, 767(1): 163-168.
[6]Dusci LJ, Peter HL, Fellows LM, Ilett KF. Determination
of olanzapine in plasma by high-performance liquid chromatography
using ultraviolet absorbance detection. J Chromatogr B Analyt
Biomed life Sci. 2002, 773(2): 191-197.
[7]Boulton DW, Markowitz JS, DeVane CL. A high-performance
liquid chromatography assay with ultraviolet detection for
olanzapine in human plasma and urine. J. Chromatogr. B., 2001,
759: 319-323.
[8] Ф�� , л��ƽ , ������ , Ҧ�� , ���� . ��ЧҺ��ɫ���ⶨ��Ѫ���аµ�ƽ��Ũ�� . ɫ�� ,
2001, 19(3): 281-283.
[9] Aravagiri M, Ames D, Wirshing WC, et al. Plasma level
monitoring of olanzapine in patients with schizophrenia: determination
by high-performance liquid chromatography with electrochemical
detection. Ther Drug Monit, 1997, 19: 307-313.
[10] Catlow JT, Barton RD, Clemens M, et al. Analysis of olanzapine
in human plasma utilizing reversed-phase high-performance
liquid chromatography with electrochemical detection. J Chromatogr
B, 1995, 668: 85-90.
[11] ���ı� , ������ , ����Ծ , ������ . ��ЧҺ��ɫ�绯ѧ��ⷨ�ⶨѪ��µ�ƽŨ�� . ҩ�������־
, 2000, 20(5): 304-307 ��
[12] ����ҩ��ίԱ�� . ҩ���Ƽ������������öȺ������Ч������ָ��ԭ�� . �л�����ҩ�� [S]. 2000
��� . ���� . ���� : ��ѧ��ҵ������ , 2000, ��¼ 193-196 ��
[13] Nyhart EH, Cenmele Jr. BJ, Kassanun K, et al. Olanzapine:
an initial assessment of the bioequivalence of capsule and
tablet formulations. Pharm Res. 1995, 12(9 suppl): S-415.
[14] Callaghan JT, Bergstrom RF, Ptak LR and Beasley CM. Olanzapine:
pharmacokinetic and pharmacodynamic profile. Drug Disposition,
1999, 37(3):177-193. |

